논리화학의 최단경로 [2]
개강 전까진 1주 2회(화/토 연재)로 바꿈.
개강후엔 쓰고싶을때 쓸듯
칼럼의 컨셉은 저번에도 말했듯이 '최단경로'임
'합리적이고 일관적이며 빠른' 풀이가 아니라 '최단경로'가 컨셉임을 유의하면 좋겠음
풀이가 좀 너무 발상적이라던가 내분을 너무 쓴다거나 그런 느낌이 들 수 있긴 할거임.
실제로도 시험장에서 모든 문제를 최단경로로 풀려고 하면 오히려 꼬이게 됨
그래도 적어도 기출문제에 한해선 최단경로 풀이를 혼자 생각해보고 알아두면 좋다고 생각해서 쓰기 시작한 칼럼임
칼럼 읽는 방법
1. 문제 사진을 보고 혼자 최단경로 풀이를 생각해본다
(혼자 안 풀어보고 풀이 감상만 하면 도움은 1도 안되고 오히려 독이 됩니다)
2. 자신의 풀이와 칼럼의 풀이를 비교 해 보고 자기가 더 빠르면 댓글로 단다
3. 혹시 최단경로 풀이를 보고 싶은 기출문제는 문항넘버나 문제 캡처한 사진을 댓글로 단다
여기서 최단경로 풀이는 답을 맞추는게 아닌 증명을 의미함
예를 들어 문제에서 케이스가 두 개면, 반대편 케이스가 틀렸다는 증명도 풀이에 들어가야함
그러니깐 잘찍어서 푸는 풀이로 풀어놓고 댓글다는 이상한 짓은 ㄴㄴ
오늘은 양적 3개, 중화 1개를 준비해옴
오늘 양적은 일차함수 그래프 유형을 컨셉으로 잡았음
비킬러는 선별하기가 애매해서 댓글로 원하는거 달아주면 그거 해 드릴게요

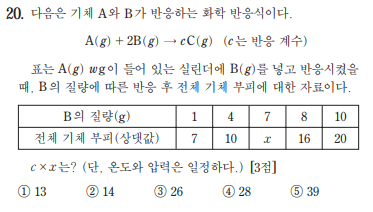
161120
스포방지용 간격
최단풀이
1. B의 질량 (1~4), (4~8), (8~10) 각각의 변화량은 3, 6, 4이고 기울기는 1, 1.5, 2임. 투입유형의 성질을 생각하면 기울기가 3개가 나오려면 (4~8)구간에 완결점이 존재함.
2. 기울기가 1, 1.5, 2 이므로 기울기를 내분 해 주면 완결점은 6(4와 8의 중점)일때임
3. 완결점 이후에 그래프 공식은 투입한 B의 질량을 t로 두면 y=2t이고, x(B질량 7)는 완결점 이후이므로 x=14
4. 기울기 공식 (c-a)/b를 사용하면 (c-1)/2:1=1:2에서 c=2. 답 28
마지막 c 구하기 다른 방법 : 완결점 이전 일차함수 공식은 y=t+6임
t=0일때 y=6, 완결점인 t=6일때 y=12이므로 전체 기체 부피 2배 -> a:c=1:2에서 c=2
추가설명
나머지는 스킵하고
기울기 내분 사용법 : 밀도 내분하듯이 기울기를 내분하면 됨
위 문제에선 기울기 1이랑 2를 걸친 평균 변화율이 1.5였으므로 1:1내분한것
물리 예시) 1차원 상의 어떤 물체가 4m/s로 운동하다가 10m/s로 속력을 바꿔 운동했는데, 평균속도가 8m/s이다. 총 운동시간이 6초라면, 4m/s로 운동한 시간은?
풀이 : 8의 4와 10에 대한 내분비는 2:1임. 따라서 시간 비는 역수이므로 1:2, 4m/s로 운동한 시간은 2초

190919
스포방지용 간격
이건 최단루트를 완벽히 이해하면 암산까지 가능한데, 대신에 중간중간 생각할게 좀 있고 일반적인 풀이 같지는 않음
최단루트
1. 그래프의 기울기가 완결점 전후 -3:1이므로 기울기 공식에 의해 a=5를 얻음.
2. 초기 부피가 y이므로, 완결점(B 5w)에서의 부피는 계수 비에 의해 2y/5
3. 반응 계수비를 보면 B:C=1:2이므로 이때까지 투입한 B의 부피는 y/5이며, 이게 5w의 부피임을 알 수 있음. 즉 B w당 부피가 y/25
4. 따라서 B 8w지점에서 전체 기체 부피는 2y/5 + 3y/25 = 13y/25. 이게 26이므로 y=50
5. B w당 부피가 y/25=2L이므로 B 20w당 부피가 40L, 즉 B 분자량 x=20w. 답은 5/2w
다른 최단루트
1. 기울기 공식에 의해 a=5
2. 0w지점에선 전체 기체 부피가 y. 계수 비에 의해 5w지점에서 전체 기체 부피는 2y/5
3. 일차함수니깐 내분으로 4w지점의 값을 구하면 됨. y와 2y/5를 4:1 내분하면 (5y+8y)/25=13y/25. 이게 26이니깐 y=50.
4. 완결점에서 부피는 20인걸 알 수 있고, B 3w를 넣었는데 6L증가했으므로 B 20w당 부피가 40L -> 분자량 20w. 답 5/2w

200720
스포방지용 간격
설명 포함 최단풀이
0. 주의할점 : 미리 반응을 어느정도 시킨 상태에서 더 반응시키는 상황임 낚이면 안됨
1. (0~w), (w~2w), (2w~3w)의 변화는 -6, -2, 2. 구간 길이 같으므로 이걸 평균 변화율로 둬도 무방하며, 기울기가 세개가 나왔으므로 앞선 문제와 같은 논리로 완결점은 (w~2w)에 존재함
2. -2는 -6과 2의 중점이므로 기울기 내분 하면 완결점은 1.5w
3. 기울기 비가 완결점 전후 -6:2=-3:1이므로, 기울기 공식을 사용하면 a=5
4. 1.5w에서 전체 기체의 부피는 완결점 이전이나 이후의 기울기를 이용해서 계산하면 12, 계수 비에 의해 시작할 때 부피는 30
5. 21은 30과 12의 중점이므로, 과정 (가)에서 1/2반응지점까지 반응시킨 후 (나)에서 계속 B를 투입했다는 것을 알 수 있음.
6. 1/2반응지점까지 반응시키려면, A의 초기 부피가 30이므로 B는 부피 3 만큼 넣어주면 됨(6개 넣으면 완결점이니깐 절반 반응지점은 3개넣으면 됨). 따라서 n/m=1/10, a랑 곱하면 1/2
요약 : 기울기공식쓰면 a=5, 내분하면 완결점 1.5w, 1.5w일때 부피 12니깐 시작할때 부피 30, 21은 30이랑 12의 중점이므로 (가)에서 1/2반응지점까지 반응시킴, 따라서 m:n=10:1. 끝.
여기까지 포인트 : 일차함수 그래프 유형은 내분을 은근 많이 쓰게 된다. 잘 분석해보자

210920
스포방지용 간격
일단 들어가기에 앞서서 이 문제는 많은 학생(심지어 강사들 마저) 논리적 비약을 하며 풀고있음
다들 첨가한 산 용액의 부피가 V일때 (나)의 몰농도가 (다)보다 작으므로 (나)가 2가를 투입했다~이런 소리를 하는데
너무 당연한 반례 하나를 들면, 만약에 이 시점에서 (나)랑 (다)가 둘 다 산성이면 작은 쪽이 1가를 투입한거임
(나)에서 V일때 염기성이니깐 가능하지 않냐고 물어볼 수 있는데
(다)가 V일때 산성이면 또 모순 만들 수 있음
제대로 된 논증은 (나)와 (다)가 둘다 염기성이다 -> 중화점 이전에 1가 산을 투입하면 이온 수는 안변하는데, 2가 산을 투입하면 개수가 감소한다->따라서 (나)가 2가를 투입했다 이거임.
암튼 최단풀이
0. 염기성 용액에 산성용액 한 종류를 일정하게 투입하면 모든 이온의 몰 농도 합 그래프는 무조건 감소하다가 증가하는 개형을 가진다는 것을 상기하자(만약 산성용액 두 종류를 투입하면 감소하다가 일정하거나, 계속 감소하는 그래프 개형을 가지는 것도 가능함)
1. (나)에서 V와 3V일때 모든 이온의 몰 농도 합이 같으므로, 개형을 떠올리면 V일때 염기, 3V일때 산성이다.
2. (다)에서 V와 2V일때 모든 이온의 몰 농도 합을 비교하면 V일때 더 크므로, V는 확실히 염기이고 2V일때 액성은 알 수 없다(만약 V가 산성이라면 2V일 때 모든 이온의 몰 농도 합은 증가해야함)
3. (나)와 (다)가 V일때 둘 다 염기성이므로, 모든 이온의 몰 농도 합이 더 작은 (나)가 2가 산을 투입한 상황이다
----------------논증파트 끝--------------------
1. (다)에서 투입한 HA가 0ml, Vml일 때 모든 이온의 개수 합이 같아야 하므로 1*10=(V+10)*3/5을 풀면 V=20/3
2. (나)에서 3V(=20)ml을 투입했을때 이온의 양은 1/2 * (20+10)=15mmol. 2가 산과 1가 염기의 혼합이고, 액성은 산성이므로 15mmol의 1/3인 5mmol이 B2-의 양
3. HA와 H2B의 몰농도가 같으므로 (다)의 3V 시점에서 A-의 양도 5mmol
4. 반응 초기에 모든 이온의 양은 10mmol이므로 Na+의 양은 5mmol임. 즉 (다)의 3V시점에서 용액은 중성. 모든 이온의 양은 여전히 10mmol
5. 따라서 10/30=1/3이 답
설명 하나 : 2가 산과 1가 염기의 혼합 상황에서 염기일때, 산성일때 모든 이온의 개수 합 공식은 그냥 외워두자
산을 x개 염기를 y개 넣었다 치면
만약 산성이면 전체 개수는 3x가되고
만약 염기면 전체 개수는 2y-x가 됨
이걸 더 확장한 공식이 있긴 한데 내책에 있음 대충 캡쳐해옴


0 XDK (+0)
유익한 글을 읽었다면 작성자에게 XDK를 선물하세요.
-
1년 쉬었으니 1월부턴 해야겠죠?
-
현역때 23수능백분위99입니다 다른과목도 마찬가지겠지만 수능문제만의 깔쌈함이있습니다...
-
만약 맞으면 새벽에도 똥 사진은 못보겟네 쩝
-
그냥 에쎈피 구매부터 시작해서 과외 한명치 수익은 주식에 쭉 쓰려고 하는데 어떤가요?
-
진짜 소신발언이긴한데 그냥 순수재미부족이었름... 물론 내기준임...
-
몇 개년 기출문제를 꼼꼼히 분석하는 사람은 공부 뿐 아니라 뭘 해도 안됩니다. 3
기출문제가 중요하다. 기출문제만 정말 열심히 돌리면 이것만으로 1등급 가능하다. 이...
-
얘 말고도 알아본 애들 더 있겠죠? ㅠㅠ
-
윤사 지2 2
나도내가왜이렇게 수능을치는지 모르겠어..
-
어디까지 되나요
-
화학 하시는분들 6
개인적으로 좋아하는 분자있음? 난 탄산수소이온 좋아함 HCO3-이거
-
이걸진짜했네 무친놈
-
서강대정도면 정말좋은학벌인데
-
헬린이 간단한 질받좀 받아주실분…..
-
인간구미호 6
ㅋㅇㅋㅌ ㅅㅇㅋ <<<<< ㄹㅇ
-
난 28년생인데 3
이상하다...
-
난 칼답잘하는데 여잔아닌것같다..
-
얼마만에 이상한 메타 안돌고 평화로운 새벽 1시야 덕분에 침대 시트에 똥도 푸짐하게...
-
배인규랑 야차룰로 현피떠서 지고 바닥에 말파e쓰는거 ㅋㅋ
-
원자력보단 경금가는 게 낫겠죠..? 물리 바보인 듯해서.... 물12 다...
-
건동홍숙 칸수 3
아직도 표본 많이 안 들어온거겠죠 크리스마스 지나면 상위 대학 말고 동숙 ~ 국숭...
-
일반고 교과 전형입니다. 1차에 30명모집에 14명 돌았는데 작년 기준 많이 돈 건가요??
-
한참 낮은 대학도 8칸밖에 안뜨는구나
-
애니 추천좀용 15
ㄱㄱ
-
그만들어오라고ㅅㅂ 나 최초합 하나는 만들고 발뻗잠하고싶은데이런
-
일단 넌 아니야 우으으으응
-
이거 진짜에요?? 메디컬라인 고속성장 연초면 진학사 5칸도 안되는건가요 의대 치대...
-
바로 자리 옮기면 기분 나빠하려나 옆자리에 누가 앉는거 진짜 끔찍히 싫어해서 맨날...
-
저는 현역때 23수능 백분위99를 맞았습니다 모든 문제유형에 해당하는것은아니지만...
-
의대떨어지면 서울대에서 1학기 휴학걸고 반수하려는거예요?? 자전에 가/다군 메디컬...
-
내일엽떡한통 다먹을예정~~
-
버그인가
-
어휴 슈붕 1
수학 실력대비 96 감사하지만 100이었으면 칸수만 보고 원서 내고 오르비가튼건 안하는건대
-
인스타 보다 개긁힘 22
대학교 1학년 아닌데~
-
최근 3년 체육교사 임용티오인데 이것도 엄청 죽은편입니다 다른 과목들은 두자리수...
-
뭐임
-
떨어질까봐 미쳐서 돌아버리겠네 맨날 등수 3등씩밀리는데 이 새기들은 어디있다가...
-
사탐런 관련질문 14
국어가1등급이 보장될 정도의 실력이 아닌경우에는 그냥 과탐에 있는게 맞는거죠??...
-
미안해애-
-
학문 개통 6
ㅋㅋㅋㅋㅋㅋ 뿌아아아앙
-
감당 가능해요?막 슬밴바키어과 같은 곳 가면 감당 못할 것 같은데저라면 그냥 한...
-
이제 기말 끝난 예비고2인데요,, 지구과학을 인강으로라도 듣는게 좋을까요? 메가패스...
-
기하 인강 0
개념은 뭔 교재로 하는게 제일 조음? 기하 노베이고 현우진 도형노베는 들었음
-
논술을 대비한다고 생각하고 겸사겸사 미적 기하 확통을 다 한다 (기하 확통은 힘...
-
언매 ebs 0
유대종 풀커리 타려고 하고 언매 들으려는데 예비 고2이면 ebs 언매 스팀팩 하는거...
-
+ 오리비와 함께 즐겁게 놀아요
-
전자공은 쓰지 마세요~~ 소문항 한개 틀리고 광탈했어요! (시립, 서강)
-
외대 논술 경제 0
빠지시는 분 계신가요 ?
-
오르비는 내 글에 댓글 못 달게 하는 기능 없음? 14
차단하고 싶은 사람이 한 명 있는데
-
어떤가요?? 1지망은 무조건 경희대긴 합니다..




















































190919 a=5 안쓰는 풀이 하나 얹자면
0,0 5w,x를 이어주면 전 후 기울기가 2:1
13w=26이 나오고, 26이 y와 20을 4:1내분점이라 y=50을 구하는 방법.
그런데 a=5가 뻔히 보이는데 안찾고 푸는게 넌센스긴 하죠 ㅋㅋ
210920 V = 20/3 안구하는 풀이 하나 얹자면
액성 구한 후
V지점에서 이온 수 비가 6:5
중화점에서 이온 수 비가 4:3이니까 1.5V에서 2가 중화 -> 3V에서 1가 중화
1가 염기에 산 용액 첨가, 혼합용액이 산성일때 전체이온수 = 첨가한 산 이온수
따라서 3V지점 이온수비는 3:2
y=1/3
그런데 위랑 마찬가지로 V=20/3이 보이는데 안구한다는게 넌센스라 너무 뒷북스러운 풀이
첫번째껀 처음보네용
두번째껀 알고는 있었는데 까먹고 안 적었네요ㅋㅋ 근데 안구하는게 넌센스긴하죠 풀이시간 비슷하기도 하고

논화!논화!논화!논화!논화!6평 18번같은 순한맛 양적 빨리 푸는 방법이 궁금해요.. 그 문제를 19번보다 더 오래걸린듯

와 너무 유익해요!